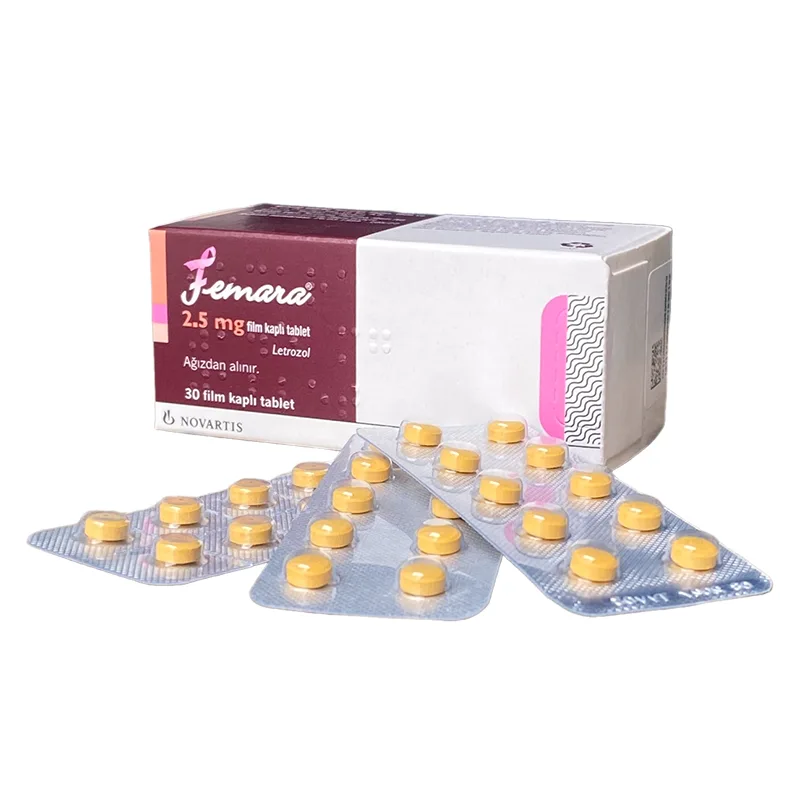
Thành phần
Letrozole: 2.5mg
Tá dược: Silic dạng keo khan, cellulose vi tinh thể, lactose monohydrat, magnesi stearat, tinh bột ngô, tinh bột natri glycollate, hydroxypropyl methylcellulose, polyethylene glycol 8000, talc, titan, dioxide (E 171), oxid sat màu vàng (E 172).
Chỉ định (Thuốc dùng cho bệnh gì?)
- Điều trị bổ trợ cho phụ nữ sau mãn kinh bị ung thư vú giai đoạn đầu, có thụ thể hormone dương tính.
- Điều trị bổ trợ kéo dài cho phụ nữ sau mãn kinh bị ung thư vú giai đoạn đầu trước đây đã được trị liệu bổ trợ chuẩn bằng tamoxifen.
- Trị liệu đầu tay cho phụ nữ sau mãn kinh bị ung thư vú tiền triển phụ thuộc hormone.
- Điều trị ung thư vú tiến triển ở phụ nữ mãn kinh tự nhiên hoặc nhân tạo, trước đây đã được điều trị với các thuốc kháng estrogen.
- Điều trị tiền phẫu thuật ở phụ nữ sau mãn kinh bị ung thư vú khu trú với thụ thể hormone dương tính, để cho phép phẫu thuật bảo tồn vú ở phụ nữ vốn không được xem là đối tượng cho loại phẫu thuật này. Điều trị tiếp tục sau phẫu thuật cần theo đúng trị liệu chuẩn.
Chống chỉ định (Khi nào không nên dùng thuốc này?)
- Quá mẫn cảm với hoạt chất hoặc với bất kỳ thành phần nào của tá dược.
- Tình trạng nội tiết tiền mãn kinh, có thai, cho con bú (Xem thêm phần 'Phụ nữ có thai và cho con bú' và 'Các dữ liệu an toàn lâm sàng').
Liều dùng
- Liều Femara được khuyến cáo là 2,5mg, 1 lần/ngày. Trong điều trị bổ trợ và bổ trợ kéo dài, nên tiếp tục dùng Femara trong 5 năm hoặc cho đến khi có tái phát khối u, tùy theo sự kiện nào đến trước. Ở bệnh nhân bị di căn, cần tiếp tục điều trị bằng Femara cho đến khi thấy rõ sự tiến triển của khối u. Không cần chỉnh liều ở bệnh nhân cao tuổi.
- Trẻ em: Không dùng thuốc này cho trẻ em.
- Bệnh nhân bị suy gan hoặc suy thận: Không cần chỉnh liều đối với bệnh nhân bị suy gan hoặc suy thận (độ thanh thải creatinine > 10 ml/phút). Tuy nhiên, cần giám sát chặt chẽ bệnh nhân bị suy gan nặng (chỉ số Child-Pugh loại C) (Xem phần 'Dược động học').
Tác dụng phụ
Nói chung Femara được dung nạp tốt qua tất cả các nghiên cứu như là một trị liệu đầu tay và trị liệu thứ hai đối với ung thư vú tiễn triển, là điều trị bổ trợ đối với ung thư vú giai đoạn đầu và điều trị bổ trợ kéo dài cho phụ nữ trước đây đã có trị liệu chuẩn bằng tamoxifen. Khoảng 1/3 bệnh nhân được điều trị bằng Femara trong nhóm có di căn và điều trị tân bổ trợ, khoảng 75% bệnh nhân trong nhóm bổ trợ (cả 2 nhóm Femara và tamoxifen, với thời gian điều trị trung bình là 60 tháng) và khoảng 80% bệnh nhân trong nhóm bổ trợ kéo dài (cả 2 nhóm Femara và giả dược, với thời gian điều trị trung bình là 60 tháng) gặp các phản ứng bất lợi. Nói chung về bản chất, các phản ứng bất lợi quan sát được chủ yếu là nhẹ hoặc trung bình, và hầu hết có liên quan với sự thiếu estrogen.
Các phản ứng bất lợi thường gặp nhất trong các nghiên cứu lâm sàng là nóng bừng, đau khớp, buồn nôn và mệt mỏi. Nhiều phản ứng bất lợi có thể quy cho là hậu quả dược lý thông thường do sự thiếu hụt estrogen (ví dụ nóng bừng mặt, rụng tóc và chảy máu âm đạo).
Các phản ứng phụ của thuốc sau đây được liệt kê trong Bảng 1 đã được báo cáo từ các thử nghiệm lâm sàng và từ kinh nghiệm hậu mãi với Femara.
Các phản ứng phụ được xếp loại theo đề mục về tần suất, đầu tiên là hay gặp nhất, sử dụng quy ước sau đây: rất hay gặp (> 1/10), hay gặp (> 1/100, < 1/10), ít gặp (> 1/1000, < 1/100), hiếm gặp (> 1/10.000, < 1/1000), rất hiếm gặp (< 1/10.000), bao gồm cả các báo cáo lẻ tẻ.
Thận trọng (Những lưu ý khi dùng thuốc)
- Các trường hợp sau đây cần hết sức thận trọng khi sử dụng:
+ Bệnh nhân loét dạ dày.
+ Bệnh nhân có bệnh thận và gan.
+ Thận trọng khi sử dụng cho bệnh nhân dưới 18 tuổi.
- Sử dụng cho phụ nữ có thai và cho con bú
Do chưa đủ các dữ kiện an toàn khi dùng cho phụ nữ có thai và cho con bú, do đó chống chỉ định khi dùng cho hai đối tượng này.
- Tác động của thuốc lên khả năng lái xe và vận hành máy móc
Do thuốc có tác dụng phụ gây ra đau đầu, chóng mặt, cần thận trọng khi dùng cho các công việc đòi hỏi sự tỉnh táo như lái xe và vận hành máy móc.
Tương tác thuốc (Những lưu ý khi dùng chung thuốc với thực phẩm hoặc thuốc khác)
- Các nghiên cứu về tương tác trên lâm sàng với cimetidine và warfarin cho thấy việc sử dụng phối hợp Femara với những thuốc này không gây ra tương tác thuốc đáng kể trên lâm sàng.
- Một đánh giá các dữ liệu của thử nghiệm lâm sàng cho thấy không có chứng cứ về các tương tác lâm sàng khác có liên quan với các thuốc thường được kê đơn khác.
- Đến nay chưa có kinh nghiệm lâm sàng về việc dùng Femara phối hợp với các thuốc chống ung thư khác.
- Letrozole ức chế in vitro, các cytochrome P459.isozyme 2A6 và ức chế vừa phải đối với 2C19. CYP 2A6 không đóng vai trò chủ yếu trong sự chuyển hóa thuốc. Trong các thử nghiệm in vitro, letrozole thực chất không thể ức chế sự chuyển hóa diazepam (một cơ chất của CYP2C19) ở nồng độ cao hơn khoảng 100 lần so với nồng độ quan sát được trong huyết tương ở trạng thái ổn định. Vì vậy, không chắc xảy ra những tương tác có liên quan trên lâm sàng với CYP2C19. Tuy nhiên, cần thận trọng khi dùng đồng thời các thuốc có khuynh hướng phụ thuộc chủ yếu vào các isoenzyme này và thuốc có chỉ số điều trị hẹp.
Bảo quản: Không bảo quản ở nhiệt độ trên 30°C. Tránh ẩm.
Đóng gói: Hộp 3 vỉ x10 viên.
Thương hiệu: Novartis
Nơi sản xuất: Thuỵ Sĩ.